Bilangan Asam (BA), Ester (BE), Penyabunan (BP), Iodin (BI), Angka, Kimia - Untuk memilih kadar suatu lemak dan ketidakjenuhan asam lemak di dalam lemak sanggup dilakukan melalui identifikasi sebagai berikut.
a. Angka / Bilangan Asam (BA)
Bilangan asam yaitu bilangan yang mengatakan berapa mg KOH yang diharapkan untuk menetralkan lemak (khususnya asam lemak bebas) dalam 1 mg lemak. Bilangan asam ditentukan dengan cara titrasi alkalimetri, yaitu teknik titrasi dengan pereaksi suatu alkali (KOH). Reaksi yang terjadi yaitu sebagai berikut.
R–COOH + KOH → R–COOK + H2O
Penentuan bilangan asam :
Keterangan :
V(KOH) = Volume basa (mL)
M(KOH) = Konsentrasi basa (M)
Mr(KOH) = Massa molekul relatif basa (g mol–1)
Untuk lebih memahami identifikasi lemak melalui bilangan asam ini, lakukan percobaan berikut.
Percobaan Penentuan Bilangan Asam (BA) suatu Lemak :
Tujuan
Menentukan kadar lemak dan ketidakjenuhan asam lemak dalam lemak.
Alat :
- Buret
- Erlenmeyer
- Statif
- Pipet tetes
Bahan :
- Lemak 2 mg
- Campuran eter dan alkohol 25 mL
- Indikator PP
- Larutan KOH 0,1 M dalam alkohol
Langkah Kerja :
- Larutkan 2 mg lemak atau minyak yang berwujud cair ke dalam 25 mL larutan dari adonan eter dan alkohol.
- Masukkan larutan tersebut ke dalam labu erlenmenyer. Kemudian, teteskan indikator PP.
- Titrasi larutan tersebut dengan larutan KOH 0,1M dalam alkohol hingga tercapai titik selesai titrasi. Amati perubahan yang terjadi.
Pertanyaan :
- Mengapa lemak atau minyak yang berwujud cair dalam percobaan ini, harus dilarutkan terlebih dulu dalam adonan eter dan alkohol?
- Mengapa dalam penentuan titik selesai titrasi perlu dilakukan penambahan indikator?
- Apa yang sanggup Anda amati ketika titik selesai titrasi tercapai?
- Jelaskan apa yang sanggup Anda simpulkan dari hasil pengamatan tersebut.
Diskusikan dengan teman kelompok Anda
Larutan hanus dibentuk dengan cara melarutkan kristal iodin dan bromin cair ke dalam asam asetat glasial.
b. Angka / Bilangan Ester (BE)
Bilangan ester yaitu bilangan yang menyatakan berapa mg KOH yang diharapkan untuk menyabunkan ester yang terdapat dalam 1 gram lemak atau minyak. Jadi, bilangan ester merupakan suatu ukuran kadar ester yang terdapat dalam minyak atau lemak.
Penetapan BE sanggup terganggu kalau dalam lemak terdapat suatu anhidrida atau suatu lakton. Teknik yang dipakai untuk mengidentifikasi bilangan ester yaitu dengan cara merefluks adonan lemak atau minyak dengan KOH berlebih, hingga terbentuk sabun. Kelebihan KOH yang ditambahkan selanjutnya dititrasi. Tahap reaksi yang terjadi yaitu sebagai berikut.
1) Trigliserida + KOH → Gliserol + R–COOK (sabun)
2) KOH (sisa) + HCl → KCl + H2O
c. Angka / Bilangan Penyabunan (BP)
Bilangan penyabunan yaitu bilangan yang mengatakan berapa mg KOH diharapkan untuk membentuk 1 gram sabun secara sempurna. Teknik yang dipakai yaitu titrasi asidimetri sesudah proses penyabunan sempurna. Teknik untuk mengidentifikasi bilangan penyabunan sama menyerupai dengan penentuan bilangan ester. Dengan cara merefluks adonan lemak atau minyak dengan KOH berlebih dan mentitrasi kelebihan KOH.
d. Angka / Bilangan Iodin (BI)
Bilangan iodin yaitu bilangan yang mengatakan berapa mg halogen (dinyatakan sebagai iodin) yang sanggup diikat oleh 100 mg lemak, atau berapa persen halogen yang sanggup diikat lemak.
Senyawa halogen yang dipakai untuk penentuan bilangan iodin yaitu senyawa antar halogen, yaitu Iodobromida (IBr, senyawa hanus). Senyawa hanus bereaksi dengan lemak melalui reaksi adisi pada ikatan rangkap. Persamaan reaksinya:
Dengan demikian, bilangan iodin merupakan ukuran banyaknya ikatan rangkap dalam asam lemak.
Teknik yang dipakai untuk memilih bilangan iodin yaitu titrasi iodometri. Titrasi dilakukan sesudah reaksi adisi berlangsung sempurna. Kelebihan bromin direaksikan dengan KI semoga terbentuk I2, selanjutnya I2 direaksikan dengan natrium tiosulfit. Reaksi keseluruhan yaitu :
Anda kini sudah mengetahui Bilangan Asam (BA), Bilangan Ester (BE), Bilangan Penyabunan (BP), dan Bilangan Iodin (BI),. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Sunarya, Y. dan A. Setiabudi. 2009. Praktis dan Aktif Belajar Kimia 3 : Untuk Kelas XII Sekolah Menengah Atas / Madrasah Aliyah. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 298.
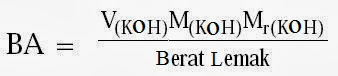
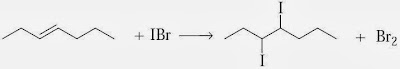
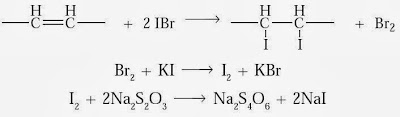
No comments:
Post a Comment