Pengertian Sabun dan Detergen, Struktur, Kegunaan, Fungsi, Pembuatan, Contoh, Kimia - Sabun ialah garam logam alkali (biasanya garam natrium) dari asam-asam lemak yang mengandung jumlah atom karbon umumnya 16 dan 18. Akan tetapi, ada juga sabun yang mengandung asam lemak dengan rantai karbon lebih pendek.
1. Sabun
Pembuatan sabun telah dilakukan semenjak masa lampau (mesir kuno). Sebelum masehi, sabun sudah dibuat dari bubuk flora yang mengandung kalium karbonat. Abu tersebut dididihkan dengan kapur (CaO) membentuk kalium hidroksida. Selanjutnya pendidihan kalium hidroksida dengan lemak binatang menghasilkan sabun. Sabun generasi pertama yang menyerupai dengan sabun kini dibuat di Italia pada tahun 600 M. Pada waktu itu bahan-bahan baku yang digunakan ialah lemak dan kalium hidroksida. Sabun yang dihasilkan tidak murni alasannya ialah memakai materi baku yang juga tidak murni.
Teknik yang dikembangkan masih primitif. Dengan ditemukan teknik pemurnian materi baku dan pemahaman yang memadai terhadap reaksireaksi kimia dalam pembuatan sabun maka pada abad-abad berikutnya dihasilkan sabun bermutu tinggi.
Sabun mandi dibuat pertama kali dari kalium hidroksida dan lemak hewan.
Praktikum / Percobaan Pembuatan Sabun
Tujuan :
Untuk menciptakan sabun dari lemak dan natrium hidroksida (NaOH).
Alat :
1. Gelas kimia
2. Gelas ukur
3. Batang pengaduk
4. Bunsen
Bahan :
1. Lemak
2. Larutan NaOH 6 M
3. Garam dapur (NaCl)
4. Air
Langkah Kerja :
1. Campurkan lemak dengan larutan NaOH 6 M. Kemudian, didihkan sambil diaduk.
2. Setelah reaksi tepat tambahkan garam dapur, dan basuh dengan air.
Pertanyaan :
1. Bagaimana persamaan reaksi dalam proses penyabunan tersebut.
2. Jelaskan mengapa perlu dilakukan penambahan NaOH 6 M.
3. Mengapa pada final reaksi perlu ditambahkan garam dapur (NaCl)?
Contoh Soal SPMB 2004
Hasil samping yang diperoleh dalam industri sabun ialah ....
A. alkohol
B. ester
C. glikol
D. gliserol
E. asam karbon tinggi
Pembahasan :
Reaksi pembentukan sabun (safonifikasi)
ester (lemak) + basa kuat→ sabun + alkohol (gliserol)
Dalam industri pembuatan sabun, ester yang digunakan ialah lemak. Jadi, alkohol yang dihasilkan berupa gliserol (CH2OH–CHOHCH2OH) merupakan hasil samping. (D)
Sabun mempunyai dua bagian, yaitu belahan ekor dan kepala. Bagian ekor berupa hidrokarbon rantai lurus, belahan kepala berupa garam natrium atau kalium dari ion karboksilat yang bersifat polar. Bagian ekor bersifat nonpolar sehingga hanya larut dalam materi yang juga non polar, menyerupai minyak atau lemak. Bagian kepala bersifat polar sehingga hanya larut dalam pelarut polar menyerupai air. Sabun yang umum digunakan ialah garam natrium atau kalium dari asam stearat atau palmitat. Struktur molekulnya ialah :
 |
| Gambar 1. Struktur molekul sabun. |
a. Sabun sebagai Pengemulsi
Jika air dan minyak dicampurkan, akan membentuk dua lapisan. Lapisan atas ialah minyak dan lapisan bawah ialah air. Jika gabungan minyak dan air dikocok, minyak akan pecah menjadi butiran-butiran yang tersebar dalam campuran. Campuran ini disebut emulsi. Emulsi minyak-air tidak stabil. Jika dibiarkan, butiran-butiran minyak akan bergabung kembali menyerupai semula membentuk lapisan minyak di atas permukaan air.
Minyak dan air jikalau dicampurkan membentuk emulsi yang tidak stabil. Setelah ditambahkan sabun, terbentuk emulsi minyak-air yang stabil. Rantai karbon larut dalam minyak, dan gugus karboksil larut dalam air.
Jika sabun ditambahkan ke dalam emulsi minyak dan air maka emulsi tersebut menjadi stabil, tidak terpisah lagi. Hal ini disebabkan oleh belahan ekor sabun akan melarutkan butiran minyak, dan belahan kepala akan berada dan larut dalam air.
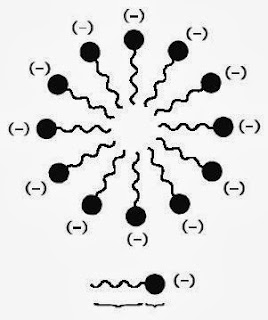 |
| Gambar 2. Misel Butiran minyak seperti dikelilingi oleh lapisan bermuatan negatif. |
Butiran-butiran minyak seperti larut dalam air dengan tunjangan sabun. Dalam hal ini, peranan sabun sanggup dijelaskan sebagai berikut.
- Bagian ekor sabun masuk (larut) ke dalam butiran minyak alasannya ialah sama-sama nonpolar.
- Bagian kepala sabun berada di luar permukaan butiran minyak alasannya ialah bersifat polar (tidak larut dalam minyak). Bagian kepala larut dalam air alasannya ialah sama-sama polar.
- Oleh lantaran belahan kepala sabun bermuatan negatif maka setiap butiran minyak seperti dikelilingi oleh satu lapisan bermuatan negatif membentuk misel (lihat Gambar 2).
- Muatan negatif yang mengelilingi butiran minyak mengadakan tolakmenolak satu sama lain sehingga butiran-butiran minyak tidak akan bergabung membentuk lapisan minyak menyerupai semula. Jadi, sabun dikatakan menstabilkan emulsi minyak-air.
b. Sabun sebagai Pencuci
Sabun biasanya garam natrium stearat atau natrium palmitat. Rumus umum sabun ialah R–COONa, dengan R ialah alkil dari hidrokarbon. Sabun yang dibuat dari garam natrium stearat, mempunyai rumus:
C17H35COONa
Jika sabun dari garam stearat dilarutkan dalam air maka akan terionisasi sebagai berikut.
C17H35COONa(aq) → C17H35COO–(aq) + Na+(aq)
Ion stearat terdiri atas dua gugus, yaitu kepala ( –COO– ) bersifat ionik dan hidrofil, serta ekor (C17H35–) bersifat hidrofob.
Tindakan sabun dalam membersihkan pakaian dari kotoran menurut pada sifat kedua ujung ion stearat ini. Secara umum tindakan sabun dalam mencuci pakaian dibagi dalam dua tahap, yaitu tahap pembasahan ( etting) dan tahap pembersihan (cleaning).
1) Tahap Pembasahan
Semua molekul air akan tarik-menarik satu sama lain. Di dalam air, kekuatan baku-tarik ini seimbang dalam segala arah. Akan tetapi, di permukaan air akan terbentuk dua arah gaya tarik yaitu gaya tarik ke arah dalam dan gaya tarik ke arah samping, menyerupai ditunjukkan pada Gambar 3.
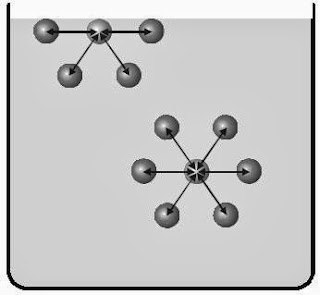 |
| Gambar 3. Tarik-menarik antar molekul air. |
Kedua arah tarikan ini mengakibatkan air mempunyai suatu gaya tegang. Gaya ini dinamakan tegangan permukaan air. Sifat dari tegangan permukaan menghalangi air untuk membasahi suatu objek yang akan dicuci. Jika sabun dicampurkan ke dalam air maka partikel-partikel sabun akan larut di dalam air dan tersebar di antara molekul-molekul air.
Penyebaran ini menurunkan gaya tarik antar molekul air. Penurunan gaya tarik ini melemahkan tegangan permukaan air. Dengan melemahnya tegangan permukaan air maka air sanggup membasahi objek yang akan dicuci dengan mudah.
2) Tahap Pencucian
Pakaian yang akan dicuci biasanya terdapat kotoran berupa lemak. Jika sabun diaduk bahu-membahu pakaian yang berlemak maka ujung hidrofob akan larut dalam lemak, sedangkan ujung hidrofil berada dalam medium air. Selama pencucian, pergerakan molekul-molekul air akan menarik belahan kepala molekul sabun, dan kepala molekul sabun akan menarik belahan ekornya. Akibat tarikan itu, belahan ekor akan menarik lemak sampai pecah dan terpisah dari permukaan pakaian.
Lemak yang terlepas dari pakaian dibawa oleh gerakan air. Kotoran yang menempel pada lemak juga akan turut lepas. Lemak bahu-membahu sabun dalam air akan membentuk emulsi.
2. Detergen
Detergen tergolong materi yang digunakan sebagai pencuci. Detergen dibagi dalam dua jenis yaitu detergen alam dan detergen sintetik. Detergen alam dibuat dari minyak binatang atau minyak sayuran menyerupai sabun mandi. Detergen sintetik biasanya dibuat dari minyak bumi. Detergen agak berbeda dari sabun. Sabun ialah garam natrium dari asam karboksilat, sedangkan detergen ialah garam natrium dari asam sulfonat, menyerupai natrium alkil sulfat dan natrium alkilbenzen sulfonat.
Sabun dan detergen mempunyai gugus fungsi berbeda. Sabun mempunyai gugus fungsi ion karboksilat (COO–), sedangkan detergen mempunyai gugus fungsi ion sulfonat (SO3–) atau ion sulfat (O–SO3–).
Bagian ekor yang telah dikembangkan untuk pembuatan detergen ialah alkil sulfat dan alkilbenzena sulfonat. Rantai alkil sulfat mengandung 10–18 atom karbon. Rantai ini berasal dari alkohol, menyerupai lauril alkohol.
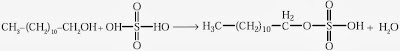
Reaksi lauril alkohol dengan asam sulfat pekat menghasilkan asam sulfonat. Asam ini selanjutnya direaksikan dengan natrium hidroksida membentuk natrium lauril sulfat. Persaman reaksinya:
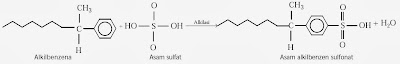
Rantai alkilbenzena sulfonat berasal dari minyak bumi. Rantai ini dibuat dari rantai alkena lurus (10–12 atom karbon) dengan cincin benzena. Alkilbenzena yang dihasilkan, lalu direaksikan dengan asam sulfat pekat membentuk asam alkilbenzen sulfonat. Selanjutnya asam ini dinetralkan oleh natrium hidroksida membentuk detergen. Contoh reaksi yang terjadi ialah sebagai berikut.
Selanjutnya, alkilbenzena direaksikan dengan asam sulfat.
Bagian ekor yang dihasilkan di atas selanjutnya direaksikan dengan natrium hidroksida membentuk detergen. Contoh:
Asam alkilbenzena sulfonat bereaksi dengan natrium hidroksida membentuk detergen natrium alkilbenzen sulfonat (ABS), sedangkan lauril hidrogen sulfat bereaksi dengan natrium hidroksida membentuk detergen natrium lauril sulfat (LAS).
Anda kini sudah mengetahui Sabun dan Detergen. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Sunarya, Y. dan A. Setiabudi. 2009. Praktis dan Aktif Belajar Kimia 3 : Untuk Kelas XII Sekolah Menengah Atas / Madrasah Aliyah. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 298.


No comments:
Post a Comment