Pengaruh Suhu Terhadap Laju Reaksi, Temperatur, Dasar Teori, Contoh Soal, Pembahasan, Praktikum Kimia - Reaksi kimia terjadi alasannya ialah adanya tumbukan yang efektif antar partikel, tumbukan yang terjadi alasannya ialah partikel-partikel yang selalu bergerak. Dengan peningkatan suhu, energi kinetik partikel semakin besar. Hal ini mengakibatkan gerak partikel juga semakin besar, sehingga kemungkinan terjadinya tumbukan yang efektif juga semakin besar. Di samping memperbesar energi kinetik, ternyata peningkatan suhu juga meningkatkan energi potensial suatu zat. Dengan semakin besarnya energi potensial zat, maka semakin besar terjadinya tumbukan yang efektif, sehingga laju reaksi semakin cepat. (gambar 1).
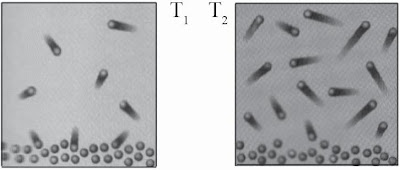 |
| Gambar 1. Gerakan partikel-partikel dalam reaksi kimia pada suhu T1 dan T2. |
Untuk memahami lebih mendalam ihwal imbas suhu terhadap laju reaksi, lakukan percobaan berikut.
Praktikum Pengaruh Suhu terhadap Laju Reaksi
Alat dan materi :
- pemanas (kompor listrik atau lampu spiritus dan kaki tiga)
- termometer
- gelas kimia 3 buah
- kertas putih yang diberi tanda silang besar
- larutan natrium thiosulfat (Na2S2O3) 0,2 M
- larutan HCl 2 M
Cara kerja :
- Masukkan masing-masing 20 mL larutan Na2S2O3 ke dalam gelas kimia. Beri tanda dengan kertas label untuk gelas kimia 1, 2, dan 3.
- Panaskan di atas kompor masing-masing gelas kimia berisi larutan Na2S2O3 sampai suhu masing-masing 25 °C, 35 °C, dan 45 °C.
- Letakkan gelas kimia tadi di atas kertas putih yang sudah diberi tanda silang.
- Masukkan 10 mL larutan HCl ke dalam masing-masing gelas kimia berisi larutan Na2S2O3 yang telah dipanaskan. Tekan pencatat waktu (stopwatch) ketika larutan HCl mulai bercampur dengan larutan Na2S2O3.
- Hentikan pencatat waktu segera sesudah tanda silang di kertas sudah tidak tampak lagi.
- Salin dan catat waktu yang dibutuhkan ke dalam tabel pengamatan.
Tabel Pengamatan
Percobaan ke | Suhu (°C) | Molaritas10 mL HCl (M) | Molaritas 20 mL Na2S2O3 (M) | Waktu (detik) |
1 | 25 | 2 | 0,2 | ........................ |
2 | 35 | 2 | 0,2 | ........................ |
3 | 45 | 2 | 0,2 | ........................ |
Bagaimana kesimpulan Anda dengan percobaan di atas?
Pada umumnya reaksi kimia akan berlangsung dua kali lebih cepat, apabila suhu dinaikkan 10 °C. Jika dimisalkan laju reaksi pada saat t1°C = v1 dan laju reaksi sesudah dinaikkan suhunya t2 °C = v2, maka laju reaksi sesudah dinaikkan suhunya atau v2 tersebut sanggup dirumuskan sebagai:
Contoh Soal Pengaruh Suhu Terhadap Laju Reaksi (1) :
Suatu reaksi berlangsung dua kali lebih cepat setiap suhunya dinaikkan 10 °C. Jika laju reaksi pada ketika suhu 20 °C ialah x M/detik, tentukan laju reaksi pada ketika suhu dinaikkan menjadi 60 °C!
Pembahasan :
Δt = (60 – 20) °C = 40 °C
v2 = 2(40/10) . x = 24 · x = 16x
Contoh Soal Pengaruh Temperatur Terhadap Laju Reaksi (2) :
Suatu reaksi kimia yang berlangsung pada suhu 30 °C memerlukan waktu 40 detik. Setiap kenaikan suhu 10 °C, reaksi akan lebih cepat dua kali dari semula. Tentukan waktu yang dibutuhkan bila suhu dinaikkan menjadi 50 °C!
Jawaban :
Δt = (50 – 30) °C = 20 °C
v1 = 1/t1 = 1/40
v2 = 2(20/10) x 1/40 = 22 x 1/40 = 4 x 1/40 = 1/10
t2 = 1/v2 = 1/(1/10) = 10 detik
Anda kini sudah mengetahui Pengaruh Suhu Terhadap Laju Reaksi. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Utami, B. A. Nugroho C. Saputro, L. Mahardiani, S. Yamtinah, dan B. Mulyani. 2009. Kimia 2 : Untuk SMA/MA Kelas XI, Program Ilmu Alam. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 274.
No comments:
Post a Comment